L'équipe ASTR
L’équipe ASTR a l’objectif de produire des connaissances en génétique pour adapter le tournesol aux enjeux de la transition agro-écologique.
Le tournesol est le 4ème oléagineux mondial et le 2ème en France. Ses faibles besoins en eau et en intrants ainsi que son cycle court lui procurent un profil écologique très intéressant. C’est une composante essentielle des futurs systèmes agricoles (Debaeke et al. 2021), ainsi sa production a augmenté de 44% depuis 10 ans (source USDA)
Principalement cultivé dans des environnments sujets à des stress hydriques, nous nous intéressons :
-
au contrôle génétique de la plasticité du rendement vis-à-vis du stress hydrique, du froid suite à un semis précoce pour éviter la sécheresse
-
aux mécanismes moléculaires impliqués dans les réponses aux stress abiotiques présents dans des systèmes de culture innovants
-
à l’impact du changement climatique sur l’attractivité du tournesol pour les pollinisateurs
Pour mener nos travaux, nous développons des ressources à trois niveaux :
Les outils de phénomique avec Phenotoul
L’équipe a créé et est toujours responsable de la plateforme de phénotypage haut-débit Heliaphen. Celle-ci fait partie de l’infrastructure locale Phenotoul (avec Agrophen au champ et TPMP en conditions contrôlées), elle-même partie de Phenome-Emphasis, infrastructure de recherche nationale qui fait partie du réseau européen EPPN Emphasis. Retrouvez la description ici[3] .
Nous collaborons étroitement avec Hiphen [4] pour le développement de pipelines de phénotypage haut-débit adaptés au tournesol et en lien avec nos thématiques de recherche.
Collaboration et partenariat : Plateforme TPMP du LIPME, UE Agro-écologie et Phénotypage des Cultures, LEPSE, MISTEA, Hiphen
Les ressources génétiques avec le CRB Tournesol
Dans le cadre de projets publics-privés, nous développons et caractérisons des populations recombinantes, NAM, des panels de diversité ou des populations de lignées d’introgression. Nous exploitons la diversité génétique naturelle présente dans le CRB Tournesol aux niveaux cultivé et sauvage pour réaliser des croisements qui particperons aux variétés de demain. Retrouvez le CRB Tournesol ici[5] .
Collaboration et partenariat : CRB Tournesol et équipe SPI du LIPME, Lidea, Limagrain, MAS Seeds, RAGT, Syngenta, Corteva
Les ressources génomiques avec l’ICSG
L’équipe participe activement au consortium de génomique international (ICSG) avec l’équipe SPI et la plateforme de bioinformatique du LIPME pour séquencer la diversité génétique du genre Helianthus et des lignées cultivées de tournesol. Nous collaborons au niveau international avec l’Université de Colombie-Britannique Vancouver et l’Université de Georgie, Athens pour mettre en commun nos compétences et produire des références génomiques pour le genre Helianthus utiles pour la recherche académique et l’innovation variétale. Vous pouvez retrouver le portail Heliagene de génomique ici[6] .
Collaboration et partenariat : Plateforme bioinfo et équipe SPI du LIPME, MAS Seeds, Lidea, RAGT, Limagrain, Syngenta, Corteva
[3] https://www6.inrae.fr/phenotoul/L-offre-de-phenotypage/Phenotypage-semi-controle
[4] https://www.hiphen-plant.com/
[6] https://www.heliagene.org/
NOS PROJETS
EU RIA HELEX
HelEx est un projet de recherche et d’innovation de 4 ans soutenu par le programme Horizon Europe de l’UE.
Le projet de 5,5 millions d’euros vise à identifier des stratégies moléculaires et génétiques permettant d’adapter la culture du tournesol au changement climatique tout en améliorant son empreinte environnementale.
L’objectif principal est de créer de nouvelles variétés de tournesol plus résistantes à la sécheresse et aux conditions climatiques extrêmes, en utilisant des variétés d’Helianthus Extremophilus.
HelEx : améliorer la résilience du tournesol face aux défis climatiques
Les stress abiotiques, en particulier la sécheresse et la chaleur, ont un impact significatif sur la physiologie et le développement des plantes et, par conséquent, sur le rendement des cultures.
En Europe, la sécheresse a un effet prononcé sur l’agriculture, notamment pour les producteurs de tournesol. Les espèces végétales sauvages, en particulier les 49 espèces d’Helianthus originaires d’Amérique du Nord, ont évolué pour résister à de tels stress.
Ces espèces ont développé des stratégies de résilience pour prospérer dans des environnements extrêmes, tels que les déserts et les zones de haute altitude. Elles restent très attractives pour les pollinisateurs, ce qui est crucial puisqu’elles sont auto-incompatibles. L’attrait du tournesol pour les pollinisateurs est conditionné par des signaux visuels et olfactifs, ainsi que par des récompenses comme le nectar et le pollen, susceptibles d’être affectées par les conditions environnementales.
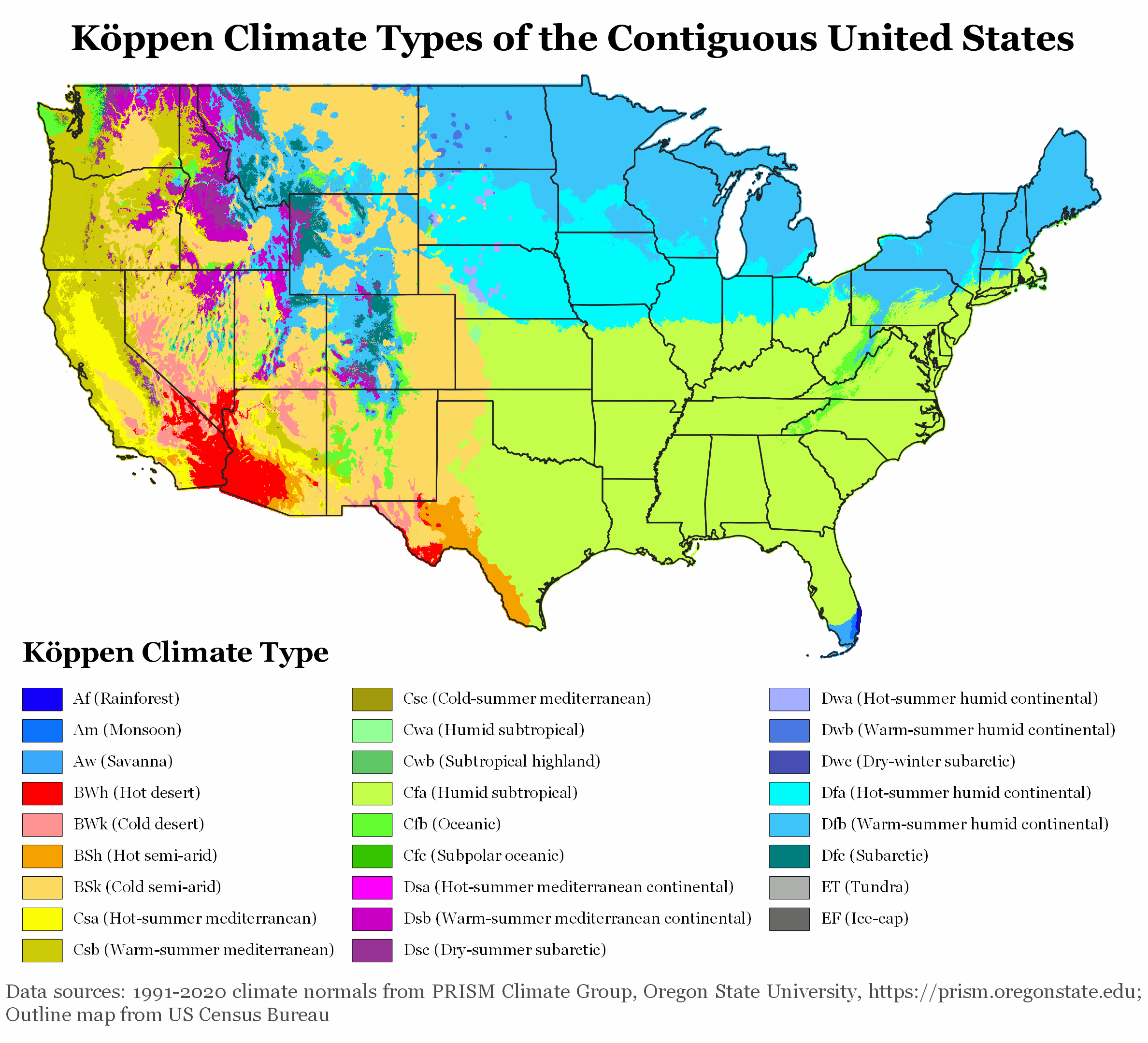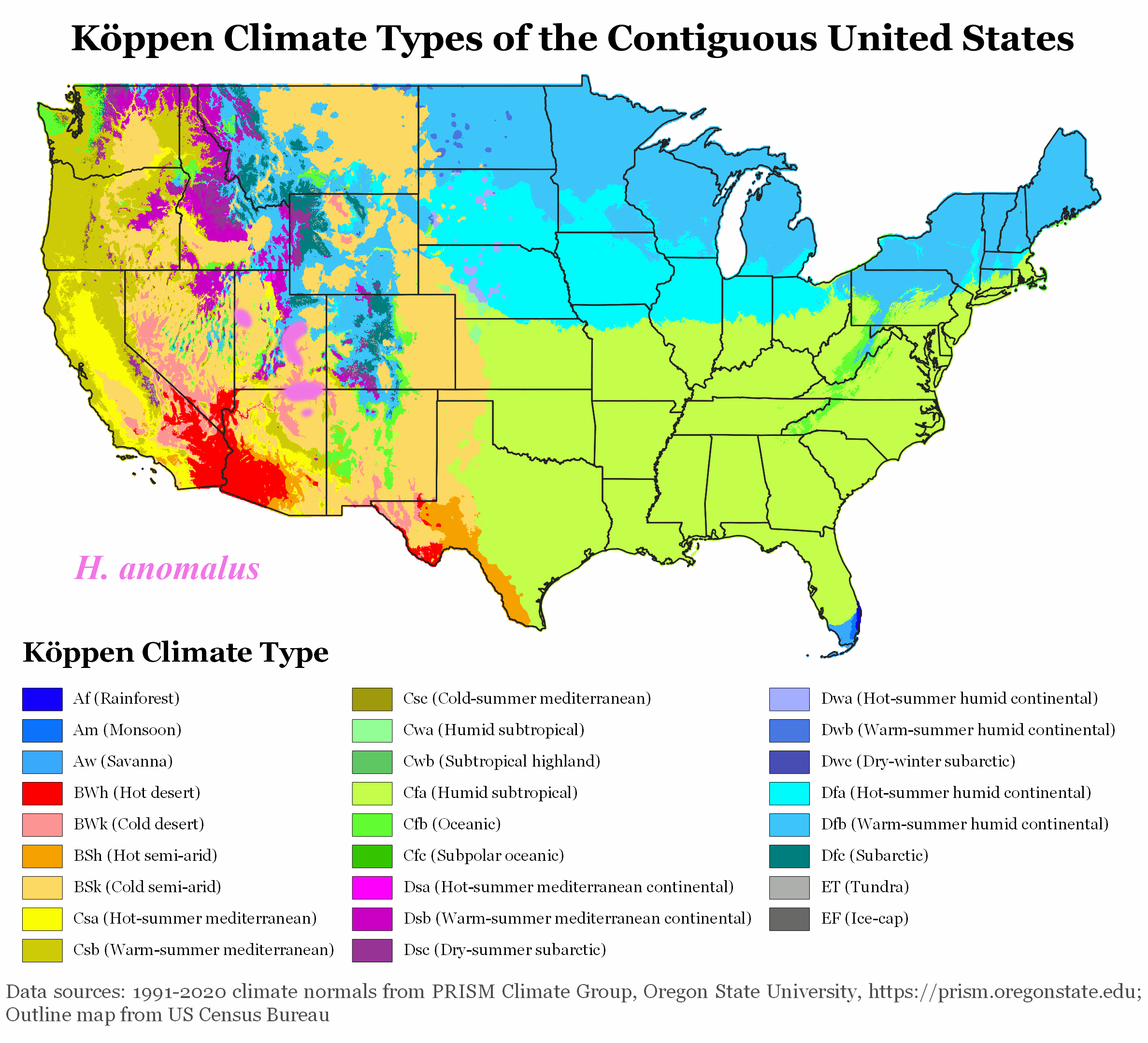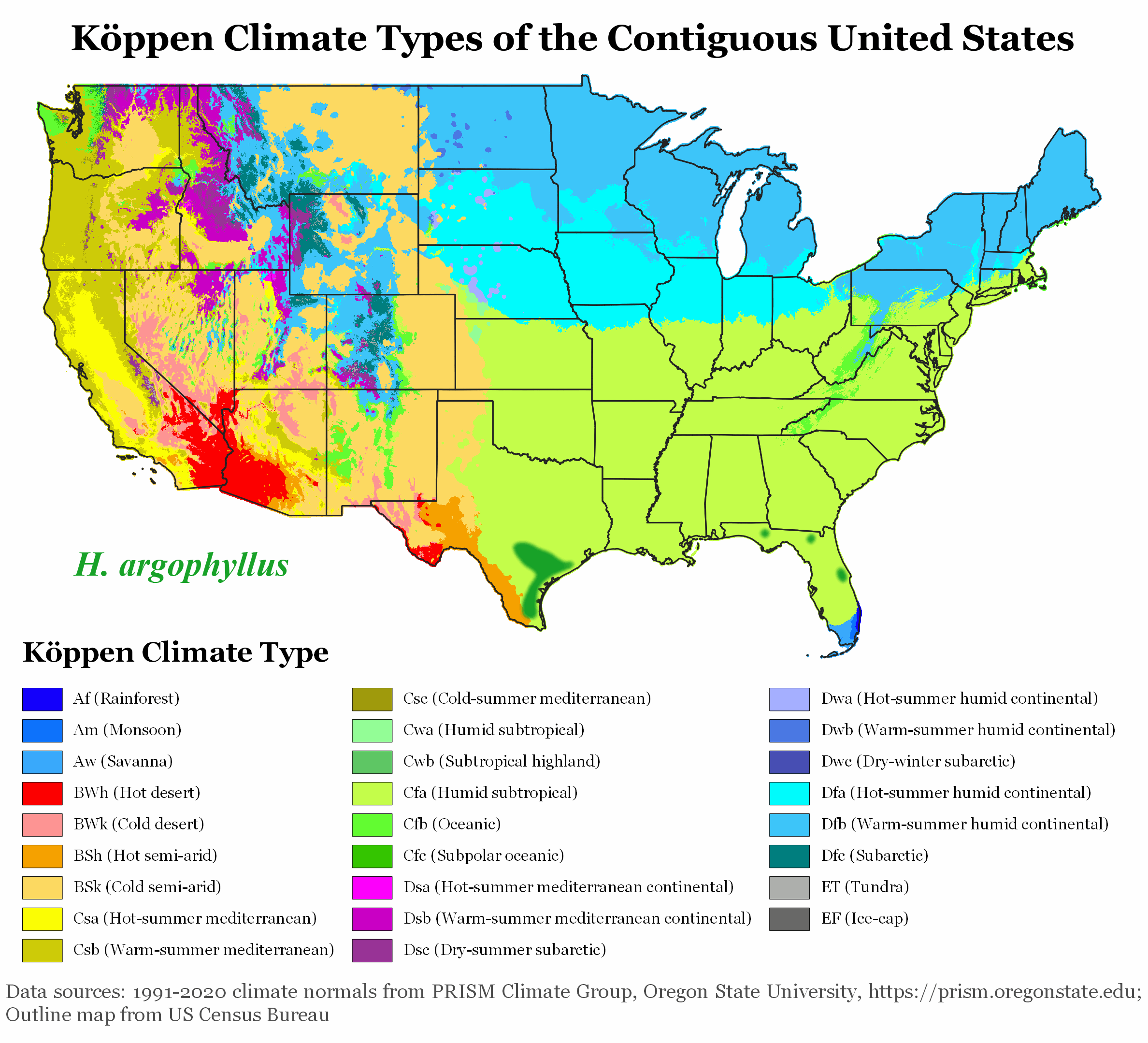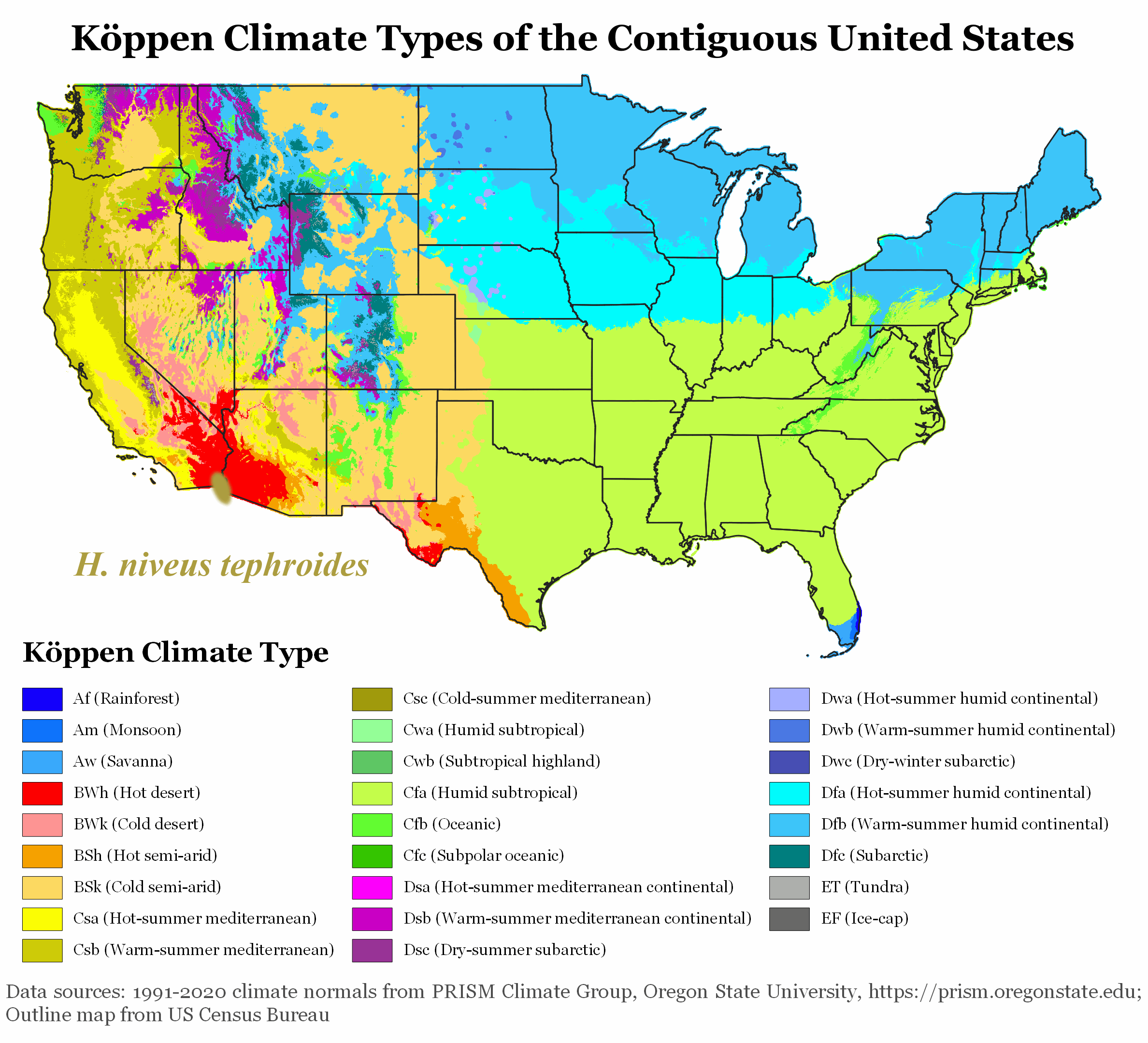

Améliorer la résilience du tournesol grâce à la génétique sauvage et aux technologies de pointe
HelEx vise à exploiter les mécanismes génétiques et moléculaires développés par les espèces sauvages d’Helianthus pour s’adapter aux climats extrêmes.
L’objectif est d’intégrer ces mécanismes dans les tournesols cultivés afin de maintenir la qualité des semences et les ressources en pollinisateurs. Plusieurs projets se sont concentrés sur la tolérance du tournesol à la sécheresse et à d’autres stress abiotiques, principalement au niveau moléculaire.
HelEx cherche à aller au-delà des connaissances existantes en développant des méthodes de phénotypage innovantes utilisant l’IA, en produisant des réseaux multi-omiques et en identifiant de nouveaux haplotypes à partir d’espèces sauvages d’Helianthus.
Le projet vise également à améliorer les programmes de sélection du tournesol, en relevant des défis tels que l’étroite base génétique du tournesol cultivé et la nature complexe des caractéristiques souhaitées.
Les 18 partenaires de HelEx
Les partenaires de HelEx associent les instituts de recherche académiques en pointe sur le tournesol et les entreprises semencières leader mondiales pour les semences de tournesol de 7 pays européens France, Allemagne, Pays-Bas, Serbie, Autriche, Roumanie, Pologne, et du Canada et des Etats-Unis.

AGRI4POL Promoting sustainable agriculture for pollinators
Les menaces pesant sur les pollinisateurs et les services de pollinisation qui soutiennent l'agriculture et apportent des bénéfices aux populations sont un problème mondial. L'ambition d'AGRI4POL est d'assister la transition de l'agriculture, en passant d'une pression sur les pollinisateurs à une force positive pour la gestion et la restauration de la biodiversité des pollinisateurs, des services de pollinisation des cultures, et des co-bénéfices pour les écosystèmes et les populations. Pour réaliser cette transition vers des systèmes agricoles et des chaînes de valeur plus favorables aux pollinisateurs, AGRI4POL fera progresser la compréhension scientifique des relations entre les systèmes de culture et les pollinisateurs, depuis le gène de la culture jusqu'à l'agroécosystème.
En évaluant la base génétique des traits floraux des cultures attirant et récompensant les pollinisateurs, nous identifierons des lignées de cultures candidates adaptées à la sélection de variétés futures intelligentes pour les pollinisateurs. Nous étudierons comment les relations entre pollinisateurs et cultures sont modifiées dans l'espace et le temps, par la diversité et la rotation des espèces et variétés de cultures, par l'infrastructure écologique (IE) comprenant des éléments paysagers et des habitats non cultivés, et par les changements climatiques ou d'utilisation des terres futurs. La synthèse de ces informations, de l'échelle génétique à celle de l'agroécosystème, nous permettra de fournir des recommandations intégrées pour optimiser les paysages en termes de pollinisation des cultures, de biodiversité des pollinisateurs et de multiples bénéfices écosystémiques.
La recherche d'AGRI4POL sera encadrée et soutenue par un engagement multi-acteurs précoce et soutenu tout au long des chaînes agroalimentaires, afin d'assurer sa pertinence et l'acceptabilité des options de gestion par les agriculteurs et la société. Cette approche multi-acteurs permettra également d'évaluer les obstacles et opportunités socio-économiques et politiques affectant la faisabilité et l'adoption d'une agriculture favorable aux pollinisateurs à des échelles [sub]nationales, européennes et internationales. AGRI4POL démontrera ainsi aux agriculteurs, aux acteurs agroalimentaires, aux décideurs politiques et à la société l'importance d'une agriculture favorable aux pollinisateurs pour la sécurité alimentaire et les objectifs de durabilité (Green Deal européen, Loi sur la restauration de la nature, ODD des Nations Unies).
Coordination : Adam Vandergen INRAE Dijon
Financement: EU Research and Innovation Action HORIZON 6M€
Partenaires : INRAE Dijon FR, INRAE Transfert Paris FR, Helmholtz-Zentrum Fur Umweltforschung Leipzig DE, The University Of Reading UK, Wageningen University NL, Stichting Wageningen Research NL, Lunds Universitet SE, CSIC Madrid ES, Albert-Ludwigs-Universitaet Freiburg DE, Pensoft Publishers BG, Ustav Vyzkumu Globalni Zmeny Av Cr Vvi Brno CZ, Universite De Mons BE, Univerza V Ljubljani SI, - University of Padova IT, WCMC LBG Cambridge UK, Associació Paisatges Vius ES, Maisadour Semences Romania SRL Belciugatele RO, CIA Padova IT, Partenaires associés: WBF Agroscope Bern CH, Agridea Fribourg CH, IARCAAS Beijing CN, China West Normal University Nanchong CN, Gansu Agricultural University Lanzhou CN
Année : 2025-2028
COPER Cold Oil yield Plasticity in sunflowER
Face au réchauffement climatique, la pratique du semis précoce apparait comme une solution efficace pour permettre aux cultures d'échapper au stress hydrique. En contrepartie, les premiers stades de développement du tournesol font faces à des températures plus basses qu’en semis traditionnel. Dans ce contexte, un travail de caractérisation phénotypique, génétique et transcriptomique à été entamé en 2021 dans le cadre du projet COPER.
Coordination : Nicolas Langlade
Financement : Contrat de collaboration bilatérale INRAE-Syngenta
Thèse associée : Jean Leconte, Université de Toulouse, Caractérisation génétique, transcriptomique et physiologique d’un QTL contrôlant la tolérance du rendement au froid chez le tournesol. Encadrement Nicolas Langlade
Année : 2019-2025
CIMS-ON
Le projet CIMS-ON, Phénotypage des variétés de cultures intermédiaires en interculture longue pour une complémentarité de services fournis au tournesol, porté par l’UMR AGIR, vise à effectuer le phénotypage de plusieurs cultures intermédiaires susceptibles de produire des services au tournesol, comme la gestion des minéraux (acquisition et restitution) et la régulation des bioagresseurs (verticillium et orobanche). L’équipe ASTR profitera du dispositif expérimental de ce projet pour étudier l’interaction entre ces cultures intermédiaires, la sénescence, la disponibilité d’azote et d’eau en fin de cycle et les bases génétiques qui pourraient jouer un rôle dans ces conditions.
Financement : Institut Carnot Plant2Pro
Coordination : Lionel Alletto (UMR AGIR)
Thèse associée : Lucie Souques, Université de Toulouse, Etude des effets abiotiques d’espèces et de variétés de cultures intermédiaires multi-services à cycle de développement sur différentes variétés de tournesol. Co-encadrement Lionel Alletto et Nicolas Langlade
IPHARD
Le projet IPHARD, Idéotypage et PHénotypage pour l’Adaptation des variétés de soja et de tournesol à la culture en Relai ou en Dérobé, vise à identifier les caractères phénotypiques du soja et du tournesol d’intérêt économique pour des conduites en relai ou en dérobé.
L’équipe ASTR participe au projet IPHARD sur le volet tournesol en dérobé pour caractériser les stress abiotiques subis par le tournesol cultivé dans cette conduite. Nous exploitons notre expertise en phénotypage de la réponse au stress hydrique sur Heliaphen pour caractériser des variétés cultivées de tournersol. Cela nous permet d’identifier quels caractères phénotypiques permettent de mieux tolérer la sécheresse et pourront être l’objet d’une sélection variétale adaptée à cette condiute de culture.
Financement : Ministère de l’Agriculture CASDAR
Coordination : Gilles Tison et Philippe Debaeke
Année : 2021-2024
Heliopollen
Le projet Heliopollen, impact du stress hydrique sur l’attractivité du tournesol vis-à-vis des insectes pollinisateurs, vise à étudier l’effet du stress hydrique sur les différents traits impliqués dans l'attractivité : morphométrie des fleurons, quantité et composition du pollen, volume du nectar et composition en sucres, et expression des gènes impliqués dans la nectarification.
Une partie fondamentale de l'étude est menée sur trois lignées sélectionnées pour leur tolérance différentielle au stress hydrique. Une partie plus appliquée mesure ces traits sur un panel d'hybrides afin d'estimer l'effet du progrès génétique sur ces traits phénotypiques en lien avec le projet Promosol Demeler.
Coordination : Olivier Catrice et Nicolas Langlade
Financement : Promosol
Année : 2021-2023
NOS PROJETS PRECEDENTS
PIA SUNRISE
Le projet SUNRISE, SUNflower Resources to Improve yield Stability in a changing Environment, a pour objectif de développer les connaissances, les ressources et les outils sur le tournesol pour permettre d’adapter cette culture aux challenges du changement climatique notamment en maintenant sa productivité dans des conditions de sécheresse.
Le projet articule plusieurs disciplines : la génétique, la génomique, la physiologie, l’agronomie et les sciences sociales. Il regroupe les acteurs de la recherche (9 laboratoires INRAE et universitaires), l’institut technique sur les oléoprotéagineux et 6 entreprises en biotechnologie et semencières dans le but non pas de travailler pour mais avec les acteurs de terrain et d’assurer un transfert plus rapide et efficace des connaissances, méthodes et ressources produites.
Le projet a un fort ancrage dans le sud-ouest et à Toulouse en particulier ce qui a renforcé la visibilité de Toulouse comme capitale mondiale de la recherche et de la sélection sur le tournesol.
SUNRISE, a constitué un projet central de l’équipe ASTR entre 2012 et 2020 et se poursuit à travers l’analyse des données produites et l’exploitation des pistes de recherches ouvertes par ce projet d’envergure.

SUNRISE EN CHIFFRES :
Budget
Total : 21M€, Subvention : 7M€ (INRAE 4.3M€), Autofinancement public : 7M€ (INRAE 4.7M€) et autofinancement privé 7M€
Financement : Agence Nationale de la Recherche ANR-11-BTBR-005
Dates : Septembre 2012 - Décembre 2020, 8 ans et 4 mois
Coordination : Patrick Vincourt (2012-2013) et Nicolas Langlade (2014-2020)
16 partenaires
-
9 laboratoires publics INRAE LIPME, INRAE AGIR, INRAE MIAT, INRAE CNRGV, INRAE EPGV, Sorbonne Université, INRAE GQE, Université Toulouse 1 LEREPS, INRAE BFP
-
1 institut technique : Terres Inovia
-
1 entreprise en biotechnologie : Innolea
-
5 semenciers : Caussade Semences puis Lidea, Mas Seeds, RAGT, , Soltis, Syngenta
Personnel
Personnel public : 86 personnes dont 32 chercheurs, 3 thèses, 10 post-docs
Personnel privé : environ 100 scientifiques
Données produites
~100 expérimentations : 45 expérimentations en champ en France, Roumanie Chili et Argentine, ~60 sur plateformes de phénotypage Phenotoul
~6700 génotypes de tournesol créés ou utilisés
7020 plantes phénotypées sur Heliaphen
>2000M de données de génotypage SNP par puces et reséquençage
~1M de données agronomiques disponibles dans la base de données SUNRISE
5M de mesures de quantité de transcrits
1.2M de niveaux de méthylation
850k mesures de quantité de métabolites
172k mesures de quantité de protéines
Résultats marquants
1 - Séquençage du premier génome de référence du tournesol en 2017 (Badouin et al ., ,2017 Nature). Issue d’une collaboration étroite du LIPME, CNRGV, GeT pour acquérir un séquenceur de nouvelle génértation et casser le verrou de l’assemblage des grands génomes complexes de plantes. Deux autres génomes du tournesol ont été séquencés ensuite dans SUNRISE. La méthodologie développée est devenue un standard en génomique a été largement réutilisée pour les séquençages de dizaines de plantes, animaux et microorganismes (rosier, Medicago, vigne, orobanche, homme, macaque, abeille, etc…).
2 – Identification du contrôle génétique de la tolérance à la sécheresse (Mangin et al.,, 2017 et Gosseau et al., 2019 et en cours de valorisation). Une approche combinée de génétique quantitative et de modélisation agronomique développée au LIPME et à AGIR et grâce aux essais des partenaires privés a permis d’identifier les types de tournesol adaptés à différents climats en Europe et aux futurs scénarios climatiques. L’intégration de ces résultats avec la modéliasation des régulations génétiques à MIAT a permis de mettre en évidence les réseaux de gènes impliqués dans la tolérance à la sécheresse qui ont été travaillés par la sélection moderne qu’il faut continuer à améliorer pour les tournersol du futur.
3- Développement d’outils de phénotypage haut-débit (Gosseau et al., 2019). Une étroite collaboration entre l’UEGCA, le LIPME et le PIA PHENOME a été permise par SUNRISE et a permis le développement des premiers outils de phénotypage haut-débit sur le tournesol appliqués sur le plus grand essai de tournesol mené à l’INRAE en 2017 (1800 parcelles sur 3ha du domaine de Langlade caractérisées en drone). Cela a également abouti à la création de l’infrastructure collective Phenotoul qui concentre sur un même site, de façon unique au monde, un continuum de la serre, à la plateforme semi-contrôlée jusqu’au champ avec TPMP, Heliaphen et Agrophen.
4 –Eco-innovations pour la filière semencière et intégration dans le système d’évaluation des variétés (Galliano et al. 2017) SUNRISE a permis de conceptualiser les éco-innovations dans le domaine de l’amélioration variétale et d’étudier les verrous de l’acceptation de ces innovations par les agriculteurs au niveau français et européen par un travail collaboratif entre AGIR et le LEREPS et en s’appuyant sur les réseaux internationaux des semenciers du projet.
5 – Développement de matériel génétique incorporant la diversité génétique sauvage. Les ressources génétiques produites dans le cadre de SUNRISE sont uniques : le Centre de Ressources Biologiques du Tournesol basé au LIPME a développé avec les partenaires semenciers 2437 lignées recombinantes, 448 lignées d’introgression avec du tournesol sauvage. SUNRISE a permis leur caractérisation moléculaire : ~3500 lignées génotypées à haute densité, ce qui prépare l’exploitation des ressources génétiques dans de futurs projets.
Nos projets antérieurs
Heliasen Analyse et phénotypage de la sénescence foliaire chez le tournesol
Coordination : Philippe Burger et Nicolas Langlade
Finacement : Promosol
Année : 2017-2020
HeliaDiv 2 Evaluation et gestion des lignées du réseau Helianthus par sélection génomique
Coordination : Brigitte Mangin
Financement : Promosol
Année : 2017-2020
HeliaDiv : Ressources génétiques du genre Helianthus : polymorphisme moléculaire et préservation de la biodiversité
Coordination : Patrick Vincourt
Financement : Promosol
Année : 2013-2016
Oleosol
Coordination : Patrick Vincourt
Financement : FUI, Midi-Pyrénées region, European Fund for Regional Development
Année : 2010-2013
Sunyfuel
Coordination : Patrick Vincourt
Financement : ANR
Année : 2008-2011
MEMBRES
Production scientifique
PhDs
Leconte, J., 2024. Caractérisation génétique, transcriptomique et physiologique d’un QTL contrôlant la tolérance au stress froid chez le tournesol cultivé Helianthus annus Université Toulouse III-Paul Sabatier, Toulouse, France.
Souques, L., 2024. Etude des effets abiotiques d’espèces et de variétés de cultures intermédiaires multi-services à cycle de développement long (7-8 mois) sur différentes variétés de tournesol. Université Toulouse III-Paul Sabatier, Toulouse, France.
Pubert, C., 2023. Caractérisation de résistances à l’orobanche du tournesol Université Toulouse III-Paul Sabatier, Toulouse, France..
Vancostenoble, B., 2022. Physiological, genetic and molecular study of the impact of water stress on the germination quality of sunflower seeds. Sorbonne Université, Paris, France.
Pegot-Espagnet, P., 2020, Utilisation de la sélection génomique dans un programme de pre-breeding : application chez la betterave sucrière. Université Toulouse III-Paul Sabatier, Toulouse, France.
Duriez, P., 2019. Caractérisation génétique, moléculaire et physiologique du locus Or7 de résistance à Orobanche cumana chez le tournesol (Doctorat). Université Toulouse III-Paul Sabatier, Toulouse, France.
Gosseau, F., 2019. Développements de nouveaux idéotypes de tournesol par une approche associant génétique et modélisation du couvert végétal (Doctorat). Université Toulouse III-Paul Sabatier, Toulouse, France.
Bonnafous, F., 2017. Prise en compte d’informations a priori en sélection génomique dans un dispositif d’hybrides de tournesol (Helianthus annuus L.) Université Toulouse III-Paul Sabatier, Toulouse, France.
Duhnen, A., 2017. Insertion de la sélection génomique dans un processus de sélection variétale : application à un oléoprotéagineux, le soja. Université Toulouse III-Paul Sabatier, Toulouse, France.
Gascuel, Q., 2014. Identification, variabilité, et connaissance in planta des effecteurs de pathogénicité de l'oomycète Plasmopara halstedii, l'agent du mildiou du tournesol. Université Toulouse III-Paul Sabatier, Toulouse, France
Marchand, G., 2014. Gene regulatory networks involved in drought stress responses : identification, genetic control and variability in cultivated sunflower, Helianthus annuus and some of its relatives. Université Toulouse III-Paul Sabatier, Toulouse, France.
As-Sadi, F., 2011. Genetic and genomic based approaches towards a better sustainability of sunflower Helianthus annuus resistance to downy mildew Plasmopara halstedii. Université Toulouse III-Paul Sabatier, Toulouse, France.
2026
Chabert, S., Cane, J.H., Vaissière, B.E., Mallinger, R.E., n.d. Are crop yields limited by pollinators? Proper assessments using pollinator gradients require measurements of flower density and yield potential. Functional Ecology n/a. https://doi.org/10.1111/1365-2435.70269
2025
Chabert, S., Mallinger, R.E., 2025. Self-sterility, self-incompatibility and xenia: a review of the mechanisms of cross-pollination benefits in animal-pollinated crops. Annals of Botany 136, 245–262. https://doi.org/10.1093/aob/mcaf047
Eeraerts, M., Siopa, C., Osterman, W., Osterman, J., Chabert, S., Verheyen, K., 2025. The Global Contribution of Wild Insect and Honeybee Visitation to Crop Pollination Success Is Asymptotic. Global Ecology and Biogeography 34, e70088. https://doi.org/10.1111/geb.70088
Husband, S., Cankar, K., Catrice, O., Chabert, S., Erler, S., 2025. A guide to sunflowers: floral resource nutrition for bee health and key pollination syndromes. Frontiers in Plant Science. 16. https://doi.org/10.3389/fpls.2025.1552335
Souques, L., Langlade, N.B., Debaeke, P., Labadie, M., Deschamps, N., Lackdari, R., Marchand, D., Lecloux, E., Tapy, C., Alletto, L., 2025. Phenotypic traits of sunflower varieties depend on the composition of cover crops. Field Crops Research 321, 109692. https://doi.org/10.1016/j.fcr.2024.109692
2024
Leconte, J.M.L., Moroldo, M., Blanchet, N., Bindea, G., Carrère, S., Catrice, O., Comar, A., Labadie, M., Marandel, R., Pouilly, N., Tapy, C., Paris, C., Mirleau-Thébaud, V., Langlade, N.B., 2024. Multi-scale characterisation of cold response reveals immediate and long-term impacts on cell physiology up to seed composition in sunflower. Plant, Cell & Environment 1-19. https://doi.org/10.1111/pce.14941
Moroldo, M., Blanchet, N., Duruflé, H., Bernillon, S., Berton, T., Fernandez, O., Gibon, Y., Moing, A., Langlade, N.B., 2024. Genetic control of abiotic stress-related specialized metabolites in sunflower. BMC Genomics 25, 199. https://doi.org/10.1186/s12864-024-10104-9
Pubert, C., Boniface, M.-C., Legendre, A., Chabaud, M., Carrère, S., Callot, C., Cravero, C., Dufau, I., Patrascoiu, M., Baussart, A., Belmonte, E., Gautier, V., Poncet, C., Zhao, J., Hu, L., Zhou, W., Langlade, N., Vautrin, S., Coussy, C., Muños, S., 2024. A cluster of putative resistance genes is associated with a dominant resistance to sunflower broomrape. Theor Appl Genet 137, 103. https://doi.org/10.1007/s00122-024-04594-0
Souques, L., Alletto, L., Blanchet, N., Casadebaig, P., Langlade, N.B., 2024. Cover crop residues mitigate impacts of water deficit on sunflower during vegetative growth with varietal differences, but not during seed development. European Journal of Agronomy 155, 127139. https://doi.org/10.1016/j.eja.2024.127139
2023
Catrice, O., Holalu, S., Terzić, S., Todesco, M., Creux, N., Langlade, N.B., 2023. Progresses of the international community to understand sunflower–pollinator interactions through multiscale approaches. OCL 30, 17. https://doi.org/10.1051/ocl/2023012
Duruflé, H., Balliau, T., Blanchet, N., Chaubet, A., Duhnen, A., Pouilly, N., Blein-Nicolas, M., Mangin, B., Maury, P., Langlade, N.B., Zivy, M., 2023. Sunflower Hybrids and Inbred Lines Adopt Different Physiological Strategies and Proteome Responses to Cope with Water Deficit. Biomolecules 13, 1110. https://doi.org/10.3390/biom13071110
Huang, K., Jahani, M., Gouzy, J., Legendre, A., Carrere, S., Lázaro-Guevara, J.M., González Segovia, E.G., Todesco, M., Mayjonade, B., Rodde, N., Cauet, S., Dufau, I., Staton, S.E., Pouilly, N., Boniface, M.-C., Tapy, C., Mangin, B., Duhnen, A., Gautier, V., Poncet, C., Donnadieu, C., Mandel, T., Hübner, S., Burke, J.M., Vautrin, S., Bellec, A., Owens, G.L., Langlade, N., Muños, S., Rieseberg, L.H., 2023. The genomics of linkage drag in inbred lines of sunflower. Proceedings of the National Academy of Sciences 120, e2205783119. https://doi.org/10.1073/pnas.2205783119
Janzen, G.M., Dittmar, E.L., Langlade, N.B., Blanchet, N., Donovan, L.A., Temme, A.A., Burke, J.M., 2023. Similar Transcriptomic Responses to Early and Late Drought Stresses Produce Divergent Phenotypes in Sunflower (Helianthus annuus L.). International Journal of Molecular Sciences 24, 9351. https://doi.org/10.3390/ijms24119351
2022
Casadebaig, P., Gauffreteau, A., Landré, A., Langlade, N.B., Mestries, E., Sarron, J., Trépos, R., Vincourt, P., Debaeke, P., 2022. Optimized cultivar deployment improves the efficiency and stability of sunflower crop production at national scale. Theor Appl Genet. https://doi.org/10.1007/s00122-022-04072-5
Lee, J.S., Jahani, M., Huang, K., Mandel, J.R., Marek, L.F., Burke, J.M., Langlade, N.B., Owens, G.L., Rieseberg, L.H., 2022. Expression complementation of gene presence/absence polymorphisms in hybrids contributes importantly to heterosis in sunflower. Journal of Advanced Research. https://doi.org/10.1016/j.jare.2022.04.008
Pomiès, L., Brouard, C., Duruflé, H., Maigné, É., Carré, C., Gody, L., Trösser, F., Katsirelos, G., Mangin, B., Langlade, N.B., de Givry, S., 2022. Gene regulatory network inference methodology for genomic and transcriptomic data acquired in genetically related heterozygote individuals. Bioinformatics 38, 4127–4134. https://doi.org/10.1093/bioinformatics/btac445
Vancostenoble, B., Blanchet, N., Langlade, N.B., Bailly, C., 2022. Maternal drought stress induces abiotic stress tolerance to the progeny at the germination stage in sunflower. Environmental and Experimental Botany 201, 104939. https://doi.org/10.1016/j.envexpbot.2022.104939
2021
Balliau, T., Duruflé, H., Blanchet, N., Blein-Nicolas, M., Langlade, N.B., Zivy, M., 2021. Proteomic data from leaves of twenty-four sunflower genotypes under water deficit. OCL 28, 12. https://doi.org/10.1051/ocl/2020074
Bengoa Luoni, S.A., Cenci, A., Moschen, S., Nicosia, S., Radonic, L.M., Sabio y García, J.V., Langlade, N.B., Vile, D., Rovere, C.V., Fernandez, P., 2021. Genome-wide and comparative phylogenetic analysis of senescence-associated NAC transcription factors in sunflower (Helianthus annuus). BMC Genomics 22, 893. https://doi.org/10.1186/s12864-021-08199-5
Berton, T., Bernillon, S., Fernandez, O., Duruflé, H., Flandin, A., Cassan, C., Jacob, D., Langlade, N.B., Gibon, Y., Moing, A., 2021. Leaf metabolomic data of eight sunflower lines and their sixteen hybrids under water deficit. OCL 28, 42. https://doi.org/10.1051/ocl/2021029
Debaeke, P., Casadebaig, P., Langlade, N.B., 2021. New challenges for sunflower ideotyping in changing environments and more ecological cropping systems. OCL 28, 29. https://doi.org/10.1051/ocl/2021016
Luoni, S.A.B., Cenci, A., Moschen, S., Nicosia, S., Radonic, L.M., Garcia, J.S. y, Langlade, N.B., Vile, D., Rovere, C.V., Fernandez, P., 2021. Genome-Wide Analysis of NAC Transcription Factors in Sunflower (Helianthus Annuus), Their Comparative Phylogenetic Analysis and Association With Leaf Senescence. BMC Plant Biology. https://doi.org/10.21203/rs.3.rs- 860249/v1
2020
Gody, L., Duruflé, H., Blanchet, N., Carré, C., Legrand, L., Mayjonade, B., Muños, S., Pomiès, L., Givry, S. de, Langlade, N.B., Mangin, B., 2020. Transcriptomic data of leaves from eight sunflower lines and their sixteen hybrids under water deficit. OCL 27, 48. https://doi.org/10.1051/ocl/2020044
Penouilh-Suzette, C., Pomiès, L., Duruflé, H., Blanchet, N., Bonnafous, F., Dinis, R., Brouard, C., Gody, L., Grassa, C., Heudelot, X., Laporte, M., Larroque, M., Marage, G., Mayjonade, B., Mangin, B., Givry, S. de, Langlade, N.B., 2020. RNA expression dataset of 384 sunflower hybrids in field condition. OCL 27, 36. https://doi.org/10.1051/ocl/2020027
Saux, M., Ponnaiah, M., Langlade, N., Zanchetta, C., Balliau, T., El-Maarouf-Bouteau, H., Bailly, C., 2020. A multiscale approach reveals regulatory players of water stress responses in seeds during germination. Plant, Cell & Environment 43, 1300–1313. https://doi.org/10.1111/pce.13731
Terzić, S., Boniface, M.-C., Marek, L., Alvarez, D., Baumann, K., Gavrilova, V., Joita-
Pacureanu, M., Sujatha, M., Valkova, D., Velasco, L., Hulke, B.S., Jocić, S., Langlade, N., Muños, S., Rieseberg, L., Seiler, G., Vear, F., 2020. Gene banks for wild and cultivated sunflower genetic resources. OCL 27, 9. https://doi.org/10.1051/ocl/2020004
2019
Fernandez, O., Urrutia, M., Berton, T., Bernillon, S., Deborde, C., Jacob, D., Maucourt, M., Maury, P., Duruflé, H., Gibon, Y., Langlade, N.B., Moing, A., 2019. Metabolomic characterization of sunflower leaf allows discriminating genotype groups or stress levels with a minimal set of metabolic markers. Metabolomics 15, 56. https://doi.org/10.1007/s11306-019-1515-4
Gosseau, F., Blanchet, N., Varès, D., Burger, P., Campergue, D., Colombet, C., Gody, L., Liévin, J.-F., Mangin, B., Tison, G., Vincourt, P., Casadebaig, P., Langlade, N., 2019. Heliaphen, an Outdoor High-Throughput Phenotyping Platform for Genetic Studies and Crop Modeling. Front. Plant Sci. 9. https://doi.org/10.3389/fpls.2018.01908
Hübner, S., Bercovich, N., Todesco, M., Mandel, J.R., Odenheimer, J., Ziegler, E., Lee, J.S., Baute, G.J., Owens, G.L., Grassa, C.J., Ebert, D.P., Ostevik, K.L., Moyers, B.T., Yakimowski, S.,Masalia, R.R., Gao, L., Ćalić, I., Bowers, J.E., Kane, N.C., Swanevelder, D.Z.H., Kubach, T., Muños, S., Langlade, N.B., Burke, J.M., Rieseberg, L.H., 2019. Sunflower pan-genome analysis shows that hybridization altered gene content and disease resistance. Nature Plants 5, 54–62. https://doi.org/10.1038/s41477-018-0329-0
Moschen, S., Marino, J., Nicosia, S., Higgins, J., Alseekh, S., Astigueta, F., Bengoa Luoni, S., Rivarola, M., Fernie, A.R., Blanchet, N., Langlade, N.B., Paniego, N., Fernández, P., Heinz, R.A., 2019. Exploring gene networks in two sunflower lines with contrasting leaf senescence phenotype using a system biology approach. BMC Plant Biology 19, 446. https://doi.org/10.1186/s12870-019-2021-6
2018
Adiredjo, A.L., Casadebaig, P., Langlade, N., Lamaze, T., Grieu, P., 2018. Genetic Analysis of the Transpiration Control in Sunflower (Helianthus Annuus L) Subjected to Drought. VEGETOS: An International Journal of Plant Research 2018. https://doi.org/10.4172/2229- 4473.1000368
Blanchet, N., Casadebaig, P., Debaeke, P., Duruflé, H., Gody, L., Gosseau, F., Langlade, N.B., Maury, P., 2018. Data describing the eco-physiological responses of twenty-four sunflower genotypes to water deficit. Data Brief 21, 1296–1301. https://doi.org/10.1016/j.dib.2018.10.045
Bonnafous, F., Fievet, G., Blanchet, N., Boniface, M.-C., Carrère, S., Gouzy, J., Legrand, L., Marage, G., Bret-Mestries, E., Munos, S., Pouilly, N., Vincourt, P., Langlade, N., Mangin, B., 2018. Comparison of GWAS models to identify non-additive genetic control of flowering time in sunflower hybrids. Theor. Appl. Genet. 131, 319–332. https://doi.org/10.1007/s00122- 017-3003-4
Xia, Q., Saux, M., Ponnaiah, M., Gilard, F., Perreau, F., Huguet, S., Balzergue, S., Langlade, N., Bailly, C., Meimoun, P., Corbineau, F., El-Maarouf-Bouteau, H., 2018. One Way to Achieve Germination: Common Molecular Mechanism Induced by Ethylene and After- Ripening in Sunflower Seeds. International Journal of Molecular Sciences 19, 2464. https://doi.org/10.3390/ijms19082464
2017
Badouin, H., Gouzy, J., Grassa, C.J., Murat, F., Staton, S.E., Cottret, L., Lelandais-Brière, C., Owens, G.L., Carrère, S., Mayjonade, B., Legrand, L., Gill, N., Kane, N.C., Bowers, J.E., Hubner, S., Bellec, A., Bérard, A., Bergès, H., Blanchet, N., Boniface, M.-C., Brunel, D., Catrice, O., Chaidir, N., Claudel, C., Donnadieu, C., Faraut, T., Fievet, G., Helmstetter, N., King, M., Knapp, S.J., Lai, Z., Le Paslier, M.-C., Lippi, Y., Lorenzon, L., Mandel, J.R., Marage, G., Marchand, G., Marquand, E., Bret-Mestries, E., Morien, E., Nambeesan, S., Nguyen, T., Pegot-Espagnet, P., Pouilly, N., Raftis, F., Sallet, E., Schiex, T., Thomas, J., Vandecasteele, C., Varès, D., Vear, F., Vautrin, S., Crespi, M., Mangin, B., Burke, J.M., Salse, J., Muños, S., Vincourt, P., Rieseberg, L.H., Langlade, N.B., 2017. The sunflower genome provides insights into oil metabolism, flowering and Asterid evolution. Nature 546, 148–152. https://doi.org/10.1038/nature22380
Bordat, A., Marchand, G., Langlade, N.B., Pouilly, N., Muños, S., Dechamp-Guillaume, G., Vincourt, P., Bret-Mestries, E., 2017. Different genetic architectures underlie crop responses to the same pathogen: the {Helianthus annuus * Phoma macdonaldii} interaction case for black stem disease and premature ripening. BMC Plant Biology 17, 167. https://doi.org/10.1186/s12870-017-1116-1
Debaeke, P., Casadebaig, P., Flenet, F., Langlade, N., 2017. Sunflower crop and climate change: vulnerability, adaptation, and mitigation potential from case-studies in Europe. OCL 24, D102. https://doi.org/10.1051/ocl/2016052
Mangin, B., Bonnafous, F., Blanchet, N., Boniface, M.-C., Bret-Mestries, E., Carrère, S., Cottret, L., Legrand, L., Marage, G., Pegot-Espagnet, P., Munos, S., Pouilly, N., Vear, F., Vincourt, P., Langlade, N.B., 2017a. Genomic Prediction of Sunflower Hybrids Oil Content. Front. Plant Sci. 8. https://doi.org/10.3389/fpls.2017.01633
Mangin, B., Casadebaig, P., Cadic, E., Blanchet, N., Boniface, M.-C., Carrère, S., Gouzy, J., Legrand, L., Mayjonade, B., Pouilly, N., André, T., Coque, M., Piquemal, J., Laporte, M., Vincourt, P., Muños, S., Langlade, N.B., 2017b. Genetic control of plasticity of oil yield for combined abiotic stresses using a joint approach of crop modelling and genome-wide association. Plant, Cell & Environment 40, 2276–2291. https://doi.org/10.1111/pce.12961
Mangin, B., Pouilly, N., Boniface, M.-C., Langlade, N.B., Vincourt, P., Vear, F., Muños, S., 2017c. Molecular diversity of sunflower populations maintained as genetic resources is affected by multiplication processes and breeding for major traits. Theor Appl Genet 130, 1099–1112. https://doi.org/10.1007/s00122-017-2872-x
2016
Andrianasolo, F.N., Casadebaig, P., Langlade, N., Debaeke, P., Maury, P., 2016. Effects of plant growth stage and leaf aging on the response of transpiration and photosynthesis to water deficit in sunflower. Functional Plant Biology 43, 797–805. https://doi.org/10.1071/fp15235
Fernandez, O., Urrutia, M., Bernillon, S., Giauffret, C., Tardieu, F., Le Gouis, J., Langlade, N., Charcosset, A., Moing, A., Gibon, Y., 2016. Fortune telling: metabolic markers of plant performance. Metabolomics 12, 158. https://doi.org/10.1007/s11306-016-1099-1
Mayjonade, B., Gouzy, J., Donnadieu, C., Pouilly, N., Marande, W., Callot, C., Langlade, N., Muños, S., 2016. Extraction of high-molecular-weight genomic DNA for long-read sequencing of single molecules. BioTechniques 61, 203–205. https://doi.org/10.2144/000114460
2015
El-Maarouf-Bouteau, H., Sajjad, Y., Bazin, J., Langlade, N., Cristescu, S.M., Balzergue, S., Baudouin, E., Bailly, C., 2015. Reactive oxygen species, abscisic acid and ethylene interact to regulate sunflower seed germination. Plant, Cell & Environment 38, 364–374. https://doi.org/10.1111/pce.12371
2014
Adiredjo, A.L., Navaud, O., Muños, S., Langlade, N.B., Lamaze, T., Grieu, P., 2014. Genetic Control of Water Use Efficiency and Leaf Carbon Isotope Discrimination in Sunflower (Helianthus annuus L.) Subjected to Two Drought Scenarios. PLoS ONE 9, e101218. https://doi.org/10.1371/journal.pone.0101218
Layat, E., Leymarie, J., El-Maarouf-Bouteau, H., Caius, J., Langlade, N., Bailly, C., 2014. Translatome profiling in dormant and nondormant sunflower (Helianthus annuus) seeds highlights post-transcriptional regulation of germination. New Phytologist 204, 864–872. https://doi.org/10.1111/nph.13002
Marchand, G., Huynh‐Thu, V.A., Kane, N.C., Arribat, S., Varès, D., Rengel, D., Balzergue, S., Rieseberg, L.H., Vincourt, P., Geurts, P., Vignes, M., Langlade, N.B., 2014. Bridging physiological and evolutionary time-scales in a gene regulatory network. New Phytologist 203, 685–696. https://doi.org/10.1111/nph.12818
Meimoun, P., Mordret, E., Langlade, N.B., Balzergue, S., Arribat, S., Bailly, C., El-Maarouf- Bouteau, H., 2014. Is Gene Transcription Involved in Seed Dry After-Ripening? PLoS ONE 9, e86442. https://doi.org/10.1371/journal.pone.0086442
2013
Cadic, E., Coque, M., Vear, F., Grezes-Besset, B., Pauquet, J., Piquemal, J., Lippi, Y., Blanchard, P., Romestant, M., Pouilly, N., Rengel, D., Gouzy, J., Langlade, N., Mangin, B., Vincourt, P., 2013. Combined linkage and association mapping of flowering time in Sunflower (Helianthus annuus L.). Theor Appl Genet 126, 1337–1356. https://doi.org/10.1007/s00122-013-2056-2
Marchand, G., Mayjonade, B., Varès, D., Blanchet, N., Boniface, M.-C., Maury, P., Andrianasolo, F.N., Burger, P., Debaeke, P., Casadebaig, P., Vincourt, P., Langlade, N.B., 2013. A biomarker based on gene expression indicates plant water status in controlled and natural environments. Plant, Cell & Environment 36, 2175–2189. https://doi.org/10.1111/pce.12127
2012
Haddadi, P., Ebrahimi, A., Langlade, N., Yazdi-Samadi, B., Berger, M., Calmon, A., Naghavi, M., Vincourt, P., Sarrafi, A., 2012. Genetic dissection of tocopherol and phytosterol in recombinant inbred lines of sunflower through quantitative trait locus analysis and the candidate gene approach. Molecular Breeding 29, 717–729. https://doi.org/10.1007/s11032-011-9585-7
Merah, O., Langlade, N., Alignan, M., Roche, J., Pouilly, N., Lippi, Y., Vear, F., Cerny, M., Bouniols, A., Mouloungui, Z., Vincourt,P., 2012. Genetic analysis of phytosterol content in sunflower seeds. Theoretical and Applied Genetics 125, 1589–1601. https://doi.org/10.1007/s00122-012-1937-0
Rengel, D., Arribat, S., Maury, P., Martin-Magniette, M.-L., Hourlier, T., Laporte, M., Varès, D., Carrère, S., Grieu, P., Balzergue, S., Gouzy, J., Vincourt, P., Langlade, N.B., 2012. A gene- phenotype network based on genetic variability for drought responses reveals key physiological processes in controlled and natural environments. PLoS ONE 7, e45249. https://doi.org/10.1371/journal.pone.0045249
Vincourt, P., As-sadi, F., Bordat, A., Langlade, N.B., Gouzy, J., Pouilly, N., Lippi, Y., Serre, F., Godiard, L., de Labrouhe, D.T., Vear, F., 2012. Consensus mapping of major resistance genes and independent QTL for quantitative resistance to sunflower downy mildew. Theoretical and Applied Genetics 125, 909–920. https://doi.org/10.1007/s00122-012-1882-y
2011
Bazin, J., Langlade, N., Vincourt, P., Arribat, S., Balzergue, S., El-Maarouf-Bouteau, H., Bailly, C., 2011. Targeted mRNA oxidation regulates sunflower seed dormancy alleviation during dry after-ripening. The Plant Cell 23, 2196-2208. https://doi.org/10.1105%2Ftpc.111.086694
Kane, N.C., Gill, N., Lindhauer, M.G., Bowers, J.E., Bergès, H., Gouzy, J., Bachlava, E.,
Langlade, N.B., Lai, Z., Stewart, M., Burke, J.M., Vincourt, P., Knapp, S.J., Rieseberg, L.H., 2011. Progress towards a reference genome for sunflower. Botany 89, 429–437. https://doi.org/10.1139/b11-032
2010
Haddadi, P., Yazdi-Samadi, B., Langlade, N., Naghavi, M., Berger, M., Kalantari, A., Calmon, A., Maury, P., Vincourt, P., Sarrafi, A., 2010. Genetic control of protein, oil and fatty acids content under partial drought stress and late sowing conditions in sunflower (Helianthus annuus). African Journal of Biotechnology 9, 6768–6782. https://hal.inrae.fr/hal-02655774v1/document



















